osteoporosi
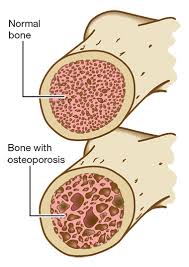
Si parla di "Osteoporosi" quando vi e’ una riduzione del tessuto osseo relativamente al volume dell’osso anatomico e quindi l’osso e’ di normali dimensioni ma contiene meno tessuto osseo.
Lo sviluppo della massa ossea può continuare fino ai 30 anni di età periodo durante il quale si costituisce un serbatoio di osso e di calcio utile per alleviare una successiva perdita ossea nel corso dell’invecchiamento. Il trascorrere del tempo infatti produce mutazioni quantitative e qualitative più o meno significative.
Si ritiene che la combinazione tra la corretta alimentazione e l’esercizio fisico in giovane età permette di rallentare questo fenomeno degenerativo.
Anche in soggetti anziani l’attività fisica contribuisce ad incrementare il contenuto minerale dell’osso e sicuramente ne rallenta la perdita.
L’osteoporosi riducendo la densità dell’osso aumenta il rischio di fratture e può colpire singoli segmenti ossei o l’intero scheletro.
Può colpire bambini ed adolescenti di entrambi i sessi ma la maggiore incidenza si ha tra le donne in pre-menopausa e gli individui sopra i 70 anni di età.
OSTEOPOROSI
L’osteoporosi è una malattia sistemica dello scheletro
caratterizzata da una ridotta massa ossea e da alterazioni
qualitative (macro e microarchitettura, proprietà materiali) che si
accompagnano ad aumento del rischio di frattura.
Sono chiamate
Osteoporosi primitive le forme di osteoporosi che compaiono
dopo la menopausa (postmenopausale) o comunque con l’avanzare
dell’età (senile).
Le Osteoporosi
“secondarie” sono quelle determinate da un ampio numero di
patologie e farmaci. L’indagine densitometrica consente oggi di
misurare in modo abbastanza accurato e preciso la massa ossea ed in
particolare la sua densità minerale (Bone Mineral Density o BMD) in
g/cm2 di superfice ossea proiettata. La BMD è responsabile della
resistenza meccanica dell’osso per il 60-80% . Per l’OMS la
diagnosi densitometrica di osteoporosi si basa sulla valutazione con
tecnica dual-energy x-ray absorptiometry (DXA) della densità
minerale, raffrontata a quella media di soggetti adulti sani dello
stesso sesso (Picco di massa ossea). L’unità di misura è
rappresentata dalla deviazione standard dal picco medio di massa
ossea (T-score). È stato osservato che il rischio di frattura inizia
ad aumentare in maniera esponenziale con valori densitometrici di
T-score < -2.5 SD che, secondo l’OMS, rappresenta la soglia per
diagnosticare la presenza di osteoporosi.
La BMD normale
è definita da un T-score compreso fra +2,5 e -1,0 (la BMD del
paziente, si colloca cioè fra 2,5 DS (deviazioni standard) sopra la
media e 1 DS sotto la media di un giovane adulto sano dello stesso
sesso.
L’osteopenia
(bassa BMD) è definita ad un T-score compreso tra -1,0 e -2,5
DS.
L’osteoporosi
è definita da un T-score inferiore a -2,5 DS.
L’osteoporosi
conclamata è definita da un T-score inferiore a -2,5 DS dalla
contemporanea presenza di una o più fratture da fragilità. Va
precisato che si tratta solo di una diagnosi densitometrica che può
essere tradotta in diagnosi clinica solo dopo una valutazione
complessiva di diagnostica differenziale. Molto utile anche la
tecnica ad ultrasuoni per l'assenza delle radiazioni, la sua facile
ripetitività ma anche per definire l'elasticità dell'osso.
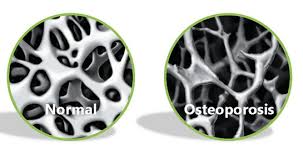
EPIDEMIOLOGIA.
L’osteoporosi rappresenta
una malattia di rilevanza sociale. La sua incidenza aumenta con l'età
sino ad interessare la maggior parte della popolazione oltre l'ottava
decade di vita. Si stima che in Italia ci siano oggi circa 3,5
milioni di donne ed 1 milione di uomini affetti da osteoporosi.
Poiché nei prossimi 20 anni la percentuale della popolazione
italiana al di sopra dei 65 anni d’età aumenterà del 25%, ci
dovremo attendere un proporzionale incremento dell’incidenza
dell’osteoporosi. Il "life time risk" di andare incontro
ad una frattura osteoporotica a carico del polso distale, dei corpi
vertebrali o del femore prossimale è di circa il 15% per ogni sito
specifico e del 40% per tutti i siti. Nella popolazione italiana con
oltre 50 anni d’età il numero di fratture di femore in un anno
supera le 90.000. Alterazioni morfologiche vertebrali sono state
riscontrate in oltre il 20% dei soggetti con oltre 65 anni d’età
di entrambi i sessi. Le fratture osteoporotiche hanno importanti
implicazioni sociali ed economiche oltre che sanitarie. I pazienti
con frattura del femore prossimale presentano entro un anno dalla
frattura, un tasso di mortalità del 15-30%. Tra gli anziani le
fratture osteoporotiche sono una delle maggiori cause di mortalità,
la cui incidenza è sostanzialmente sovrapponibile a quella per ictus
e carcinoma mammario e superiore di 4 volte a quella per carcinoma
endometriale. Il 50% delle donne con frattura di femore presenta,
inoltre, una consistente riduzione del livello di autosufficienza
che, in circa il 20% dei casi, comporta l’istituzionalizzazione a
lungo termine.
FATTORI DI
RISCHIO
La rilevanza clinica dell’osteoporosi è
legata alla riduzione della resistenza ossea con conseguente aumento
del rischio di frattura da fragilità per traumi considerati a bassa
energia. I traumi a bassa energia sono generalmente rappresentati da
cadute accidentali dalla posizione eretta o semplici attività della
vita quotidiana. Nel caso delle cadute, la probabilità di frattura
dipende dalle caratteristiche della caduta, dalla efficacia delle
reazioni protettive e dalla possibile attenuazione dell’energia del
trauma mediata dallo spessore dei tessuti molli. Tutti i fattori che
condizionano il rischio di caduta tendono ovviamente ad aumentare il
rischio di frattura. La patogenesi della frattura deve quindi tenere
conto dei molteplici fattori che influenzano sia resistenza ossea sia
frequenza e tipo di trauma. Il rischio di frattura osteoporotica è
determinato da una combinazione di fattori che agiscono
prevalentemente attraverso una riduzione della BMD e fattori
parzialmente o totalmente indipendenti dalla BMD (caratteristiche del
tessuto osseo non valutabili attraverso la BMD e fattori extraossei).
La distinzione non è ovviamente rigida e molti fattori di rischio
agiscono con più meccanismi contemporaneamente. Tra i numerosi
fattori associati in maniera indipendente al rischio di osteoporosi e
fratture che risultano di particolare importanza vanno annoverati
l’età, le pregresse frattura da fragilità, la familiarità per
fratture da fragilità, la terapia cortisonica e tutte le condizioni
che aumentano la probabilità di cadute. Inoltre, la presenza di
malattie concomitanti accentua il rischio di frattura. Nei soggetti
con più fattori di rischio il rischio di frattura è superiore a
quello di soggetti con un singolo fattore di rischio, compresa una
isolata riduzione della BMD. Di conseguenza, la valutazione della BMD
è adeguata per la diagnosi di osteoporosi (soglia diagnostica) ma
l’identificazione di soggetti ad alto rischio di frattura in cui è
appropriato un trattamento farmacologico specifico (soglia
terapeutica) richiede la combinazione di BMD e fattori di rischio
indipendenti.
I principali fattori di rischio sono:
-
Densità
minerale ossea (BMD) La riduzione della BMD è un importante
fattore di rischio di frattura. La BMD dipende dal picco di massa
ossea raggiunto all’apice dello sviluppo e dalla perdita ossea
correlata a menopausa e invecchiamento ed è influenzata da fattori
genetici e nutrizionali, abitudini di vita, malattie coesistenti e
varie terapie farmacologiche . Numerosi studi epidemiologici
prospettici, per la maggior parte effettuati misurando la BMD con
tecnica DXA nelle sedi assiali (collo del femore, femore totale e
vertebre lombari), hanno accertato che ogni riduzione di una
deviazione standard della BMD aumenta il rischio di frattura di
1.5-3 volte.
-
Età
L’incidenza di fratture osteoporotiche aumenta esponenzialmente
con l’età. il rischio di frattura correlato all’avanzare
dell’età è solo parzialmente mediato dalla riduzione della BMD,
ma dipende in gran parte da altri fattori, quali alterazioni
qualitative della struttura ossea, aumento della frequenza di cadute
e rallentamento delle risposte protettive. Un identico T-score ha un
significato diverso alle differenti età e a parità di BMD il
rischio di frattura è più elevato negli anziani rispetto ai
giovani.
-
Pregresse
fratture Una pregressa frattura da fragilità è un
importante fattore di rischio per ulteriori fratture in entrambi i
sessi. Anche se una pregressa frattura è spesso correlata a ridotta
BMD, il rischio di nuove fratture è in gran parte indipendente da
questa. Gli studi epidemiologici più recenti hanno dimostrato che
qualsiasi pregressa frattura, indipendentemente dalla sede, aumenta
il rischio di nuove fratture, anche se in misura diversa.
Particolare rilevanza prognostica va data alle fratture di vertebre
(comprese le fratture morfometriche), polso, femore e omero. Il
rischio dipende inoltre dal numero di pregresse fratture. Soggetti
con 3 o più fratture hanno un rischio di nuove fratture circa 10
volte superiore a chi non ha avuto fratture e 2-3 volte superiore a
chi ha avuto una sola frattura.
-
Familiarità
La familiarità per fratture influenza il rischio di frattura in
modo indipendente dalla BMD. In particolare la familiarità per
fratture di femore nei genitori aumenta significativamente
soprattutto il rischio di fratture del femore e, anche se in misura
minore, di tutte le fratture osteoporotiche.
-
Comorbidità
Numerose condizioni patologiche si associano a un aumento del
rischio di frattura. In molte di queste condizioni si ritiene che il
rischio sia mediato dalla riduzione della BMD. Tuttavia, spesso
entrano in gioco meccanismi diversi, tra cui infiammazione cronica,
alterazioni della qualità ossea, compromissione dello stato
generale di salute, complicanze specifiche, riduzione della
mobilità, riduzione della massa e forza muscolare (sarcopenia) e
aumento del rischio di caduta. La carenza di vitamina D spesso
associata rappresenta un ulteriore fattore negativo. Tra le
patologie vanno ricordate artrite reumatoide e altre connettiviti,
diabete, broncopneumopatia cronica ostruttiva, malattie
infiammatorie croniche intestinali, AIDS, Parkinson, sclerosi
multipla, condizioni associate a grave disabilità motoria. In
particolare,i soggetti con diabete di tipo 1 o di tipo 2 tendono a
fratturarsi a livelli di BMD superiori a quelli dei soggetti non
diabetici e il rischio di frattura è quindi parzialmente
indipendente dalla BMD.
-
Terapie
farmacologiche I farmaci per cui è stato descritto un
aumento del rischio sono numerosi. Ben noto da tempo l’effetto
osteolesivo dei glucocorticoidi, mediato in gran parte da fattori
indipendenti dalla densità ossea, anche se la terapia steroidea
induce sicuramente una rapida riduzione della BMD. Tra i farmaci di
più recente introduzione particolare menzione va riservata alle
terapie di blocco ormonale adiuvante (inibitori dell’aromatasi
nelle donne operate per carcinoma della mammella, agonisti del GnRH
negli uomini con carcinoma prostatico). Questi farmaci provocano una
progressiva riduzione della BMD, ma non è escluso l’intervento di
fattori indipendenti sul rischio di frattura. La valutazione
complessiva del rischio di frattura La valutazione integrata di BMD
e dei più importanti fattori di rischio clinici parzialmente o
talmente indipendenti dalla BMD consente una stima più accurata del
rischio di fratture da fragilità nel medio termine (5-10 anni
successivi), e l’identificazione di soggetti in cui un trattamento
farmacologico è più appropriato.
Riassumendo
a) Fattori di
rischio per osteoporosi e/o fratture osteoporotiche • Età •
Sesso femminile • Basso indice di massa corporea • Pregressa
frattura da fragilità (in particolare vertebre, comprese le fratture
morfometriche, polso, femore e omero) • Familiarità per frattura
di femore/vertebre • Fumo (in atto) • Alcool (3 o più unità/die)
• Carenza di Vitamina D • Menopausa prima dei 45 anni • Ridotta
attività fisica • Immobilizzazione protratta • Ridotto introito
di calcio • Eccessivo introito di sodio • Malattie associate ad
osteoporosi • Trapianti • Farmaci
b) Fattori di
rischio per cadute Anamnesi positiva per cadute precedenti o
Condizioni con compromissione di Forza e massa muscolare (sarcopenia)
Funzionalità arti inferiori Equilibrio Capacità visiva o
Deterioramento cognitivo o Aritmie o Farmaci (farmaci attivi sul SNC,
antipertensivi, alcol) o Deficit muscolare da ipovitaminosi D •
Fattori ambientali o Ostacoli, illuminazione, superfici, calzature
OSTEOPOROSI SECONDARIE
L’osteoporosi
postmenopausale-senile va sempre distinta dalle forme di osteoporosi
secondaria. Numerose sono le condizioni potenzialmente in grado di
provocare la comparsa di osteoporosi: trattasi di molteplici malattie
o di farmaci :
1) Elenco delle
malattie associate ad osteoporosi: Malattie endocrine: -
Ipogonadismo - Ipercortisolismo - Iperparatiroidismo - Ipertiroidismo
- Iperprolattinemia - Diabete mellito tipo I e II - Acromegalia -
Deficit GH Malattie ematologiche: - Malattie mielo e
linfoproliferative - Mieloma multiplo - Mastocitosi sistemica -
Talassemia - Gammopatie monoclonali - Anemia falciforme - Emofilia
Malattie apparato gastro-enterico: - Epatopatie croniche - Cirrosi
biliare primitiva - Morbo celiaco - Malattie infiammatorie croniche
gastro-intestinali - Resezione gastro-intestinale - Bypass gastrico -
Intolleranza al lattosio - Malassorbimento intestinale -
Insufficienza pancreatica Malattie reumatiche: - Artrite reumatoide -
LES - Spondilite anchilosante - Artrite psoriasica - Sclerodermia -
Altre connettiviti Malattie renali: - Ipercalciuria idiopatica renale
- Acidosi tubulare renale - Insufficienza renale cronica Malattie
neurologiche: - Parkinson - Sclerosi Multipla - Paraplegia Linee
Guida per la Diagnosi, Prevenzione e Terapia dell’Osteoporosi 11 -
Esiti di ictus - Distrofie muscolari Malattie genetiche: -
Osteogenesi Imperfetta - Ehlers-Danlos - Sindrome di Gaucher -
Glicogenosi - Ipofosfatasia - Emocromatosi - Omocistinuria - Fibrosi
cistica - Sindrome di Marfan - Sindrome di Menkes - Porfiria -
Sindrome di Riley-Day Altre Malattie: - Broncopneumopatia cronica
ostruttiva - Anoressia nervosa - AIDS/HIV - Amiloidosi - Sarcoidosi -
Depressione
2) Farmaci
Osteopenizzanti
GLUCOCORTICOIDI : Idrocortisone,
prednisone ,desametasone ecc. Per inibizione attività
osteoblastica/apoptosi osteocitaria;
INBITORI DELL’AROMATASI: Letrozolo,
anastrozolo, examestane. Per ipogonadismo;
SSRI * Citalopram,
fluoxetina,paroxetina. Per inibizione proliferazione osteoblastica;
INIBITORI POMPA PROTONICA:
Esomeprazolo, omeprazolo,lansoprazolo ecc.A casua di riduzione
dell'assorbimento intestinale di calcio;
H2 INIBITORI :Ranitidina, cimetidina lo
stesso come sopra;
TIAZOLIDINEDIONI: Rosiglitazone,
pioglitazone in quanto creano inibizione della neoformazione e
differenziazione osteoblastica;
ORMONI TIROIDEI (eccesso): Levotiroxina
per causa di un aumento del turnover osseo;
ANTICOAGULANTI: Eparina,warfain
Riduzione dell’attività di osteocalcina ANTICONVULSIVANTI:
Fenobarbital,acido valproico, oxacarbazepina,fentoina Interferenza
con metabolismo vitamina D
Gnrh: Leuprolide, Goserelin
Ipogonadismo con alto turnover
DIURETICI DELL’ANSA: furosemide
Effetto calciurico
AGENTI ANTIRETROVIRALI: Efavirenz,
nevirapina Tenofovir Inibitori delle proteasi Interferenza con
metabolismo vitamina D Deplezione renale di fosfato Inibizione
osteoblastogenesi
INIBITORI DELLA CALCINEURINA:
Ciclosporina A (alte dosi) ,tacrolimus Elevazione turnover osseo.
NUTRIZIONE PARENTERALE incerto
SSRI: selective serotonin reuptake
inhibitors; GnRH: gonadotropin-realising hormones; : Ci sono evidenze
di associazione con rischio di frattura .
OSTEOPOROSI MASCHILE
L’osteoporosi rappresenta un problema
di salute pubblica anche nei maschi. Circa il 20% di tutte le
fratture di femore si verifica nel sesso maschile e l’incidenza di
fratture vertebrali è circa la metà rispetto a quelle nella
femmina. Tuttavia mortalità e morbilità per frattura vertebrale e
di femore sono più elevate rispetto alla femmina. L’osteoporosi
maschile è frequentemente secondaria (circa due/terzi nei maschi
contro un/terzo nelle donne) per cui vanno sempre escluse condizioni
patologiche associate all'osteoporosi. Le cause secondarie più
comuni nel maschio sono ipogonadismo, alcoolismo, mieloma multiplo,
iperparatiroidismo, malassorbimento ed uso di corticosteroidi. In
soggetti maschi con pregresse fratture da fragilità l’indagine
densitometrica serve a confermare il dubbio diagnostico di
osteoporosi. In maschi senza frattura la misurazione della massa
ossea mediante tecnica DXA rimane il metodo di scelta per la
definizione di rischio di frattura . Una valutazione mediante DXA
della massa ossea è giustificata nei maschi in qualunque età se in
presenza di un fattore di rischio maggiore (ad esempio frattura da
fragilità, uso di corticosteroidi). Viene consigliata inoltre in
tutti i soggetti tra i 50 e i 69 anni in presenza di 2 o più fattori
di rischio minori. I principali fattori di rischio per frattura del
maschio sono sovrapponibili a quelli riscontrati nel sesso femminile
e cioè fratture da fragilità, familiarità per frattura
osteoporotica, terapie o patologie osteopenizzanti. Secondo le linee
guida americane ed inglesi l’esecuzione della DXA risulta
cost-effective sopra i 70 anni . Per l’utilizzo della tecnica ad
ultrasuoni (QUS) i dati relativi alla popolazione maschile sono
simili a quelli ottenuti nella popolazione femminile. Nei maschi
viene consigliata l’esecuzione di una radiografia della colonna
dorso-lombare per valutare la presenza di cedimenti vertebrali
prevalenti nei soggetti sopra i 50 anni con anamnesi positiva per
fratture, perdita di altezza superiore ai 4 cm rispetto all’altezza
a 20 anni o trattamento con glucocorticoidi (recente o in corso). Ne
viene inoltre suggerita l’esecuzione nei maschi tra i 70 e 79 anni
se T-score a livello vertebrale o femorale < -1,5 oppure se sopra
gli 80 anni con T-score < -1. Le linee guida NOF consigliano un
trattamento farmacologico nei soggetti che abbiano avuto una frattura
vertebrale (sia clinica che morfometrica) o femorale, nei soggetti
con osteoporosi alla DXA (T-score < -2,5 a livello vertebrale o
femorale) e nei maschi sopra i 50 anni con rischio di frattura
secondo il FRAX a 10 anni di femore > 3% o di fratture maggiori
>20%. In Italia per l’osteoporosi maschile idiopatica e
secondaria a corticosteroidi sono registrati due aminobisfosfonati
orali, l’alendronato ed il risedronato, ed uno
endovena, l’acido zoledronico (Raccomandazione di grado A). Tra le
altre classi di farmaci sono indicati denosumab (osteoporosi
idiopatica maschile ed osteoporosi iatrogena nel carcinoma della
prostata) e ranelato di stronzio. Per la forma idiopatica
maschile è, inoltre, registrato il teriparatide (20 mgc sc/die) per
le forme di osteoporosi severa (come definito dalla Nota 79) od in
presenza di nuove fratture vertebrali o femorali in corso di
trattamento con gli altri farmaci in nota 79. I farmaci con evidenza
di effetto antifratturativo nel maschio sono i bisfosfonati
(alendronato, risedronato, acido zoledronico) e il
teriparatide.
L’alendronato e il risedronato
sono in grado di aumentare la massa ossea a livello vertebrale e
femorale e di ridurre il rischio di fratture vertebrali
nell’osteoporosi maschile primitiva ed in quella indotta da
glucocorticoidi . Non vi sono dati sulle fratture non vertebrali . Lo
zoledronato ha dimostrato di migliorare la massa ossea a
livello vertebrale e femorale e di ridurre il rischio di nuove
fratture sia nell’osteoporosi maschile idiopatica che
nell’osteoporosi da glucocorticoidi. Denosumab è in grado
di aumentare la BMD nei maschi ad alto rischio di frattura ed è
indicato nel trattamento della perdita ossea nei soggetti in terapia
di deprivazione androgenica per carcinoma della prostata. Il ranelato
di stronzio ha dimostrato un incremento della massa ossea nei maschi
trattati rispetto a placebo. Il teriparatide è in grado di
incrementare significativamente la BMD al rachide e al femore e di
ridurre le fratture vertebrali medio-severe. Nell’osteoporosi da
glucocorticoidi la teriparatide risulterebbe più efficace
alla terapia con alendronato o risedronato nell’aumentare la BMD e
nel ridurre le fratture vertebrali. Non vi è evidenza di trattamenti
che nel maschio riducano il rischio di fratture non vertebrali. Il
profilo di safety dei farmaci è risultato sovrapponibile per
tipologia di eventi avversi e per incidenza degli stessi a quello
registrato nella popolazione femminile post-menopausale .
Per tutte queste terapie va garantito
un’adeguato introito di calcio (1000-1200 mg/die) e di vitamina D
(colecalciferolo 800-1000 UI /die), adesso anche sotto la forma di
spray orale per ottimizzare assorbimento.
RACCOMANDAZIONI GENERALI L’osteoporosi
maschile è frequentemente secondaria e vanno pertanto escluse le
principali forme patologiche che possono determinare osteoporosi.
E’ raccomandato il controllo della
BMD nei maschi con almeno un fattore di rischio maggiore o con età
superiore ai 50 anni e almeno due fattori di rischio minori o sopra i
70 anni anche in assenza di altri fattori di rischio per frattura
(raccomandazione di grado A) Il cut-off diagnostico densitometrico
per la definizione di osteoporosi nel maschio è un livello di
T-score < -2,5 DS rispetto al soggetto giovane adulto
(raccomandazione di grado B)
A supporto di tutte le terapie
farmacologiche va garantito un’adeguato introito di calcio e
vitamina D In Italia per l’osteoporosi maschile sono registrati
alendronato, risedronato, zoledronato, denosumab e ranelato di
stronzio (raccomandazione di grado A). Nell’osteoporosi maschile da
glucocorticoidi sono registrati alendronato, risedronato e
zoledronato (raccomandazione di grado A). In caso di osteoporosi
severa come definito dalla nota 79 o in presenza di nuove fratture
vertebrali o femorali dopo 1 anno di terapia con altri farmaci in
nota 79, è indicato trattamento con teriparatide (raccomandazione di
grado A).